Vous vous demandez si les stratégies nutritionnelles pour améliorer les performances en trail mettent en danger vos dents ? Cet article est pour vous !

Performance optimale, santé bucco-dentaire compromise ?
Les recommandations actuelles en nutrition d’endurance sont claires, je vous les ai déjà vulgarisées de nombreuses fois (dont ici). Pour soutenir l’intensité et retarder la fatigue, vos apports glucidiques à l’effort devraient être réguliers, parfois élevés, parfois jusqu’à 90 g par heure. Et pour atteindre ces recommandations, on utilise des gels, des boissons isotoniques, des barres énergétiques. Pourtant, depuis une dizaine d’années, une question a émergé dans la littérature scientifique et petit à petit dans le débat public. Ces stratégies nutritionnelles sont-elles compatibles avec une bonne santé bucco-dentaire ?
En effet, une exposition répétée aux glucides, souvent sous forme liquide ou collante, associée à des boissons acides et à une déshydratation fréquente pendant l’effort, pourrait théoriquement favoriser l’érosion de l’émail, les caries ou les maladies parodontales. Broad et Rye (2015) ont d’ailleurs posé la question de manière explicite, en nommant leur article “Do current sports nutrition guidelines conflict with good oral health”. En français ça nous donne “Les recommandations en nutrition sportive entrent-elles en conflit avec la santé bucco-dentaire ?”.
Chez le traileur, cette interrogation est importante. Les formats prolongés, l’alimentation fractionnée toutes les vingt à trente minutes et la difficulté de maintenir une hygiène buccale en course constituent un environnement singulier. Faut-il alors voir dans la stratégie glucidique moderne un risque silencieux pour la santé à long terme ? Et si oui, comment y réagir ? Faut-il faire comme Courtney Dauwalter et se brosser les dents aux ravitaillements ?
Avant de tirer des conclusions hâtives, il est nécessaire de revenir aux mécanismes biologiques, d’examiner les données épidémiologiques disponibles chez les athlètes d’endurance, et d’analyser ce que montrent réellement les essais cliniques.
C’est quoi la santé bucco-dentaire ?
La santé bucco-dentaire ne se résume pas à l’absence de carie. Elle correspond à un état d’équilibre fonctionnel et biologique de l’ensemble des tissus de la cavité orale : dents, émail, dentine, gencives, os alvéolaire, muqueuses et microbiote oral.
Selon la définition proposée par la Fédération Dentaire Internationale, la santé orale est un état permettant de manger, parler et interagir socialement sans douleur, inconfort ni infection, et sans altération progressive des structures dentaires ou parodontales. C’est en tout cas la définition actuelle, proposée par la Fédération Dentaire Internationale (FDI) en 2016, dans l’article de Glick et al. Leur définition inclut donc plusieurs dimensions : l’intégrité de l’émail, l’absence de lésions carieuses actives, un parodonte sain (c.-à-d. gencives et os sains), et un environnement microbien (microbiote buccal) équilibré.
Dans le contexte sportif, on peut imaginer une dimension spécifique à cette définition. Une atteinte bucco-dentaire peut entraîner douleur, inflammation chronique, recours aux antalgiques ou aux antibiotiques, et dans certains cas altérer la récupération ou la disponibilité à l’entraînement. La santé orale va donc participe à la santé générale et potentiellement à la performance.
Carie, érosion et maladies parondontales
Pour analyser plus précisément l’impact éventuel des stratégies nutritionnelles en endurance, trois atteintes doivent être distinguées : la carie dentaire, l’érosion de l’émail et les maladies parodontales.
Qu’est-ce qu’une carie ?
La carie est une maladie multifactorielle d’origine bactérienne. Comme le rappellent Moynihan et Petersen (2004) dans leur revue de littérature, elle résulte de la déminéralisation de l’émail et de la dentine (c.-à-d. tissu situé juste sous l’émail) par des acides organiques produits par les bactéries de la plaque dentaire à partir des sucres alimentaires. Lorsque des glucides fermentescibles sont ingérés, des bactéries telles que Streptococcus mutans les métabolisent et produisent principalement de l’acide lactique. Cette production d’acides entraîne une chute du pH au niveau de la plaque dentaire.
Lorsque le pH descend en dessous d’un seuil critique d’environ 5,5, la structure minérale de l’émail commence à se dissoudre. On parle d’hydroxyapatite de l’émail. L’émail est constitué en grande partie d’un cristal très dur appelé hydroxyapatite, composé de calcium et de phosphate. Lorsque l’environnement devient trop acide, ces minéraux quittent progressivement la surface de la dent. C’est ce qu’on appelle la déminéralisation (Moynihan & Petersen, 2004).
Qu’est-ce qu’une érosion dentaire ?
L’érosion dentaire, en revanche, ne dépend pas de l’activité bactérienne. Il s’agit d’une perte chimique irréversible de tissu dentaire liée à l’exposition directe à des acides extrinsèques (boissons acides, jus de fruits, sodas) ou intrinsèques (reflux, vomissements). Les mêmes auteurs soulignent que toute boisson ou aliment dont le pH est inférieur à 5,5 peut potentiellement induire une érosion de l’émail.
Qu’est-ce qu’une maladie parodontale ?
Les maladies parodontales concernent les tissus de soutien de la dent, c’est-à-dire les gencives, le ligament parodontal et l’os alvéolaire. Contrairement à la carie, qui affecte directement les tissus durs de la dent (émail et dentine), les atteintes parodontales touchent les structures qui maintiennent la dent en place.
La forme la plus fréquente est la gingivite. Il s’agit d’une inflammation superficielle de la gencive, généralement provoquée par l’accumulation de plaque bactérienne au niveau du collet dentaire. Elle se manifeste par des gencives rouges, gonflées et parfois saignantes. À ce stade, l’atteinte est réversible si l’hygiène est améliorée.
Lorsque l’inflammation persiste, elle peut évoluer vers une parodontite. Cette forme plus sévère entraîne une destruction progressive de l’os et du ligament qui soutiennent la dent. À long terme, elle peut conduire à une mobilité dentaire, voire à la perte de dents.
Contrairement à la carie, les maladies parodontales ne dépendent pas directement de la consommation de sucres, mais plutôt de la composition du microbiote oral, de la réponse inflammatoire de l’hôte et de la qualité de l’hygiène bucco-dentaire. Elles constituent néanmoins un enjeu majeur, car l’inflammation chronique locale peut avoir des répercussions systémiques.
Le rôle central de la salive
Un élément primordial à connaitre et comprendre pour la suite des discussions concerne la salive. Elle salive constitue l’un des principaux systèmes de défense de la cavité buccale. Moynihan et Petersen (2004) lui décrivent trois fonctions majeures.
- Premièrement, elle exerce un effet tampon grâce aux bicarbonates et autres systèmes de régulation, ce qui permet de neutraliser les acides produits par les bactéries après ingestion de sucres.
- Deuxièmement, elle participe à la clairance des substrats (c.-à-d. la capacité pour un tissu ou un organe d’éliminer une substance). Elle fait cela en facilitant l’élimination mécanique des résidus alimentaires et en réduisant le temps de contact entre les glucides et la surface dentaire.
- Troisièmement, elle favorise la reminéralisation. Saturée en calcium et en phosphate à pH physiologique, elle permet la redéposition minérale sur les zones initialement déminéralisées.
La carie apparaît lorsque la déminéralisation dépasse la capacité de reminéralisation. Il s’agit d’un équilibre dynamique, influencé par la fréquence des agressions acides, la qualité de l’hygiène bucco-dentaire, l’exposition au fluor et les caractéristiques individuelles de la salive.
Fréquence d’exposition, un déterminant majeur ?
Un des points les plus robustes de la littérature scientifique concerne l’importance de la fréquence d’exposition aux sucres libres. Moynihan et Petersen (2004) rappellent que les données issues d’études interventionnelles humaines, animales et épidémiologiques convergent vers une association convaincante entre la fréquence de consommation de sucres libres et le risque de carie. Cette dernière semble jouer un rôle au moins aussi déterminant que la quantité totale consommée.
Les auteurs soulignent qu’une consommation de sucres libres supérieure à quatre fois par jour est associée à une augmentation marquée du risque carieux. Cette notion est centrale pour comprendre le contexte de l’ultra-endurance. En trail long ou en ultra, les apports sont souvent fractionnés toutes les vingt à trente minutes pendant plusieurs heures, ce qui correspond à une succession d’épisodes potentiels d’acidification.
Cependant, le lien entre sucres et carie n’est pas mécanique ni isolé. Il est modulé par l’exposition au fluor, le niveau d’hygiène bucco-dentaire, le débit salivaire et les comportements individuels. Autrement dit, un environnement à risque ne conduit pas systématiquement à une pathologie si des mécanismes de protection efficaces sont présents.
Pourquoi s’intéresser à la santé bucco-dentaire des athlètes ? Les arguments de Engels-Deutsch
Dans sa revue publiée dans Research in Sports Medicine, Engels-Deutsch (2026) détaille les mécanismes par lesquels une atteinte bucco-dentaire peut dépasser la cavité orale et s’inscrire dans une dynamique systémique. Autrement dit, une infection ou une inflammation dentaire ne reste pas toujours confinée à la bouche.
Inflammation locale, impact systémique
Les maladies parodontales (gingivite, parodontite) correspondent à des infections chroniques des tissus de soutien de la dent. Elles s’accompagnent de la libération de médiateurs pro-inflammatoires. La CRP (protéine C-réactive) est un marqueur sanguin mesurant le niveau d’inflammation dans l’organisme. Plus elle est élevée, plus l’organisme est en état inflammatoire.
Dans le cas d’une parodontite chronique, cette inflammation locale peut entraîner une élévation mesurable de ces marqueurs dans la circulation sanguine. Il ne s’agit pas d’une infection généralisée massive, mais d’une inflammation chronique de bas grade. Par ailleurs, la gencive constitue une barrière biologique. Lorsqu’elle est fragilisée, notamment en cas d’inflammation, des bactéries buccales peuvent passer transitoirement dans la circulation sanguine lors du brossage, de la mastication ou de soins dentaires. Ce phénomène est appelé bactériémie transitoire.
Athlète et inflammation : un effet cumulatif ?
L’exercice intense est lui-même un stimulus inflammatoire physiologique. Après une séance exigeante, certains marqueurs inflammatoires augmentent temporairement, ce qui fait partie du processus normal d’adaptation. La question posée par Engels-Deutsch (2026) est donc la suivante : si un athlète présente déjà une inflammation chronique d’origine bucco-dentaire, celle-ci pourrait-elle s’additionner à l’inflammation induite par l’entraînement ?
L’auteur évoque l’hypothèse d’un effet cumulatif susceptible d’affecter :
- la récupération.
- la perfusion microvasculaire (c’est-à-dire la qualité de la circulation sanguine dans les petits vaisseaux).
- la fonction endothéliale (le bon fonctionnement de l’endothélium, la fine couche de cellules tapissant l’intérieur des vaisseaux sanguins, essentielle pour la vasodilatation et la régulation du flux sanguin).
Ce sont des mécanismes biologiquement plausibles, mais les preuves directes d’un impact mesurable sur la performance restent limitées.
Microbiote oral, nitrates et oxyde nitrique
Un autre axe discuté dans la revue concerne le rôle du microbiote oral dans le métabolisme des nitrates. Certaines bactéries présentes dans la bouche transforment les nitrates alimentaires en nitrites. Ces nitrites peuvent ensuite être convertis en oxyde nitrique, une molécule clé impliquée dans la vasodilatation, c’est-à-dire la capacité des vaisseaux sanguins à se dilater pour augmenter le flux sanguin vers les muscles.
En endurance, cette voie nitrate-nitrite participe à l’efficacité de la perfusion musculaire. Une dysbiose parodontale (c.-à-d. un déséquilibre du microbiote oral en faveur de bactéries pathogènes) pourrait théoriquement altérer cette capacité de réduction des nitrates. Là encore, il s’agit d’une hypothèse physiologiquement cohérente, mais qui reste à confirmer par des études interventionnelles solides.
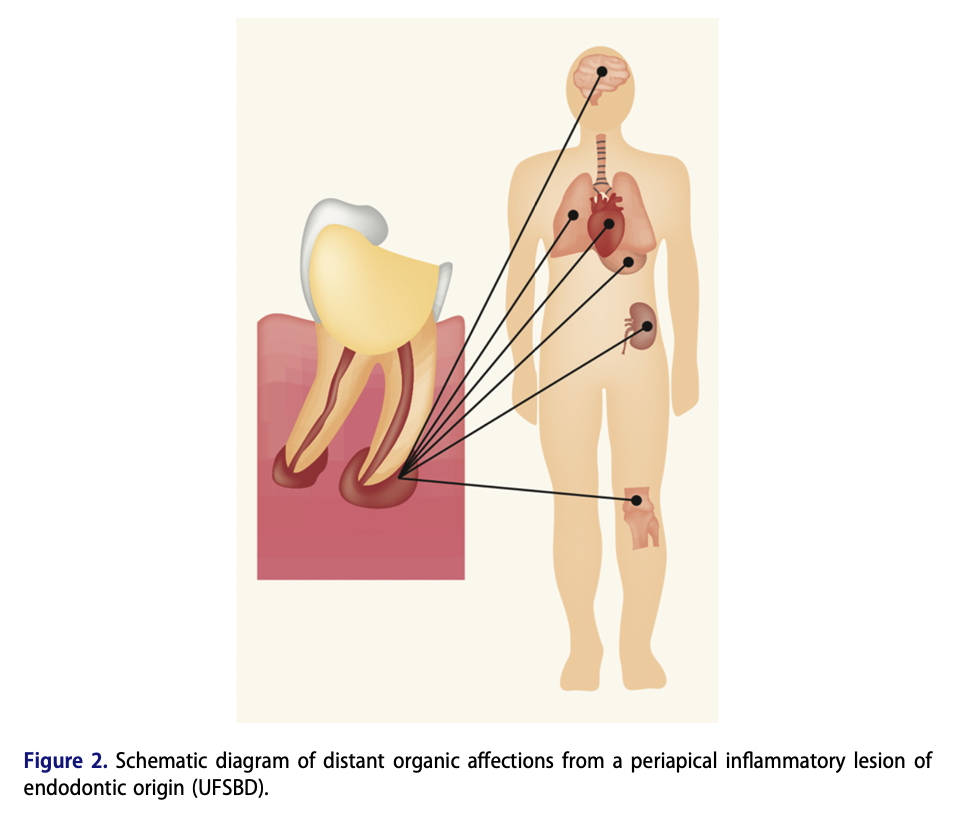
Les foyers infectieux dentaires chroniques
Enfin, Engels-Deutsch rappelle que les lésions des dents, endodontiques, chroniques constituent des foyers inflammatoires persistants. Une lésion endodontique correspond à une infection située à l’intérieur de la dent, au niveau de la pulpe, souvent secondaire à une carie profonde. Le traitement endodontique (plus connu sous le nom de “traitement de canal”) vise à éliminer cette infection interne. Certaines études citées dans la revue rapportent une diminution de la CRP après traitement endodontique réussi, suggérant que la résolution d’un foyer infectieux dentaire peut réduire l’inflammation systémique mesurable.
L’exercice d’endurance modifie-t-il l’environnement buccal ?
Avant même de parler de gels, de boissons isotoniques ou de brossage de dents en ravitaillement, il faut revenir à la base. L’exercice d’endurance peut, à lui seul, modifier plusieurs paramètres qui protègent habituellement la cavité buccale. Ce qui signifie que la stratégie glucidique, dont nous parlerons ensuite, ne s’insère pas dans un environnement neutre. Elle s’inscrit dans un contexte physiologique particulier, marqué par le stress, l’hyperventilation, la déshydratation et des variations du débit salivaire.
Données cliniques chez des triathlètes
En 2014, Frese et al. ont comparé 35 triathlètes s’entraînant au moins cinq heures par semaine à 35 individus non sportifs. Les auteurs ont réalisé un examen clinique standardisé, incluant l’évaluation des caries et de l’érosion dentaire, ainsi que des mesures salivaires.
Le premier résultat marquant est que les triathlètes présentent un risque d’érosion significativement plus élevé que les individus du groupe contrôle. Le score BEWE (Basic Erosive Wear Examination), qui quantifie l’usure érosive, était significativement supérieur chez les athlètes, les plaçant en moyenne dans une catégorie de risque modéré. En revanche, aucune différence significative n’a été observée concernant la prévalence globale des caries entre les deux groupes. Autrement dit, à un instant donné, le nombre de dents cariées, manquantes ou obturées était comparable chez les triathlètes et les non-sportifs.
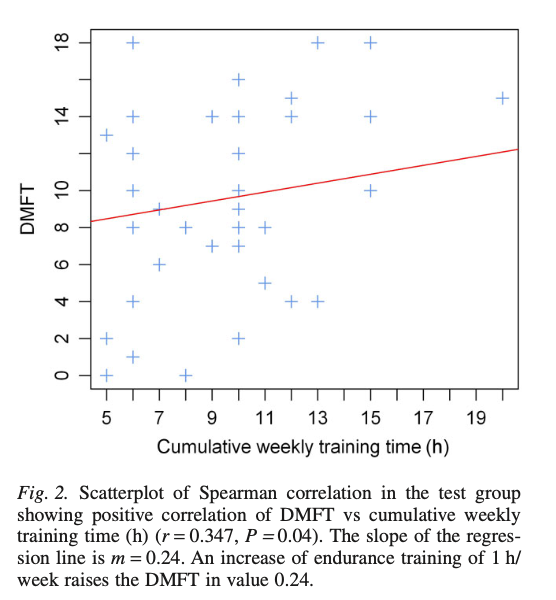
Cependant, au sein du groupe des triathlètes, le volume hebdomadaire d’entraînement était corrélé positivement au quantité de caries. Plus la charge d’entraînement cumulée était élevée, plus l’indice carieux tendait à augmenter. Ce résultat, bien que corrélationnel et non causal, suggère qu’un volume d’entraînement important pourrait s’accompagner d’une exposition cumulative plus marquée à des facteurs de risque bucco-dentaires.
Et les aliments à l’effort ?
Un point intéressant de cette étude concerne la consommation de produits sucrés de nutrition sportive. Dans le groupe des triathlètes, 74 % déclaraient consommer régulièrement des gels, barres ou boissons énergétiques. On pourrait donc s’attendre à ce que cette variable explique directement l’augmentation du risque observé. Pourtant, les analyses en sous-groupes ne montrent pas de différence significative des indices carieux ou érosifs entre les triathlètes consommateurs de produits d’effort et ceux n’en consommant pas.
Autrement dit, au sein même du groupe sportif, la variable « prise de nutrition sportive » ne semble pas associée indépendamment à une augmentation mesurable du risque carieux ou érosif. Cela suggère que le risque ne dépend probablement pas d’un produit isolé, mais plutôt d’un ensemble de facteurs cumulés, comme fréquence d’exposition, la durée d’effort, l’ampleur de la diminution du débit salivaire, les contraintes d’hygiène en situation d’entraînement ou de compétition, et la répétition des épisodes au fil des années.
Modifications salivaires à l’effort : un terrain potentiellement plus vulnérable
Toujours dans l’étude de Frese et al. (2014), un sous-groupe de 15 triathlètes a réalisé un test incrémental de course. Les auteurs ont mesuré les paramètres salivaires avant, pendant et après l’effort. Les résultats montrent une diminution significative du débit salivaire, à la fois pour la salive stimulée et non stimulée, lorsque l’intensité augmente. Cette baisse est cohérente avec l’activation du système nerveux sympathique et la redistribution du débit sanguin vers les muscles actifs.
De plus, le pH salivaire augmentait au pic d’effort dans ce protocole. Ce point est important. Il signifie que l’environnement buccal à l’effort n’est pas simplement soumis à une acidification directe. Cependant, une réduction du débit salivaire signifie mécaniquement :
- Moins d’effet tampon.
- Moins de dilution des acides.
- Moins de clairance des sucres.
Ainsi, même si le pH salivaire mesuré ponctuellement n’est pas plus bas, la capacité globale de défense peut être temporairement diminuée. Ces données suggèrent que l’exercice, indépendamment des apports nutritionnels, peut créer un environnement buccal transitoirement plus fragile.
Microbiote oral et pratique sportive
La revue systématique de Dubois et al. (2025) a analysé les données disponibles sur la relation entre pratique sportive et microbiote oral. Cinq études répondaient aux critères d’inclusion. Les travaux montrent que la pratique sportive est associée à des différences de composition bactérienne par rapport aux non-sportifs. Le genre Streptococcus est celui le plus fréquemment rapporté comme modifié, avec des variations observées dans quatre des cinq études incluses. Certaines études décrivent également une augmentation relative de genres tels que Rothia, Veillonella ou Stenotrophomonas, ainsi qu’une diminution de Gemella.
Cependant, ces observations doivent être interprétées avec prudence. Les effectifs sont faibles et hétérogènes : athlètes d’endurance, sportifs amateurs, disciplines variées, niveaux d’entraînement différents. Les méthodes d’analyse microbiologique diffèrent également selon les études, ce qui limite la comparabilité des résultats. De plus, plusieurs facteurs confondants majeurs ne sont pas systématiquement contrôlés, comme l’alimentation, l’exposition aux glucides fermentescibles, hydratation, ou encore l’hygiène bucco-dentaire. Il est donc difficile d’attribuer les différences observées à la pratique sportive seule.
Sur le plan biologique, certaines observations méritent néanmoins discussion. L’augmentation relative de genres comme Veillonella, par exemple, est intéressante. En effet, ces bactéries utilisent le lactate comme substrat énergétique. En contexte d’exercice, où la concentration de lactate augmente, on pourrait théoriquement envisager des interactions métaboliques locales. Toutefois, cette hypothèse reste spéculative.
Enfin, aucune des études incluses ne démontre un lien direct entre modifications microbiennes et risque clinique. Les auteurs concluent donc explicitement qu’il n’existe pas, à ce stade, de preuve scientifique permettant de déterminer si les variations observées du microbiote oral chez les sportifs ont un impact clinique favorable ou défavorable.
Les apports glucidiques à l’effort : un facteur de risque ?
À ce stade, une question devient inévitable. Si l’exercice modifie déjà l’environnement buccal et que la fréquence d’exposition aux sucres est un déterminant majeur du risque carieux, que disent réellement les données concernant les boissons et produits de nutrition sportive sucrés ? Une revue récente s’est penchée spécifiquement sur cette question. Il s’agit de celle de Memon et al. (2025). Les auteurs ont analysé les études disponibles évaluant le lien entre consommation de boissons sportives et érosion dentaire chez des athlètes.
Un potentiel érosif théorique indiscutable
Sur le plan physico-chimique, les boissons de l’effort présentent plusieurs caractéristiques susceptibles d’endommager l’émail. La majorité d’entre elles affichent un pH compris entre 3,1 et 3,7, donc largement en dessous du seuil critique d’environ 5,5 à partir duquel l’hydroxyapatite de l’émail commence à se dissoudre. Autrement dit, ces boissons sont chimiquement acides.
Mais le pH ne suffit pas à lui seul à prédire le risque. L’acidité titrable, c’est-à-dire la quantité totale d’acide qu’une boisson peut libérer avant d’être neutralisée, joue également un rôle central. Une boisson peut avoir un pH modéré mais une forte capacité à maintenir un environnement acide dans le temps. De nombreuses boissons isotoniques contiennent de l’acide citrique. Or cet acide peut se lier au calcium. Concrètement, il capte les ions calcium présents dans l’émail, ce qui fragilise davantage la structure minérale et ralentit la reminéralisation.
Donc sur le plan théorique, le risque érosif est réel.
Les boissons et gels d’efforts détruisent-elles vos dents ?
C’est ici que les choses deviennent intéressantes. La revue de Memon et al. (2025) a inclus cinq études transversales menées chez différents profils de sportifs. Plusieurs d’entre elles ne retrouvent aucune association statistiquement significative entre la consommation de boissons sportives et la présence d’érosion dentaire.
Chez des sportifs universitaires dont plus de 90 % déclaraient consommer régulièrement des boissons d’effort, aucune relation n’a été observée entre la quantité ingérée et les scores d’érosion. De même, dans l’échantillon des athlètes des Jeux Olympiques de Londres 2012, aucune association globale n’a été mise en évidence entre consommation et érosion. Une analyse plus fine a toutefois suggéré une relation possible sur certaines surfaces dentaires spécifiques, ce qui montre que le signal n’est pas totalement absent non-plus.
À l’inverse, deux études rapportent une association significative. Une étude norvégienne décrit une relation dose–réponse. Plus la consommation quotidienne de boissons acides est élevée, plus le risque d’érosion augmente. Une étude portugaise retrouve également une augmentation du risque chez les athlètes consommateurs de boissons énergétiques, avec des odds ratios élevés, notamment chez les nageurs. Les résultats sont donc hétérogènes.
Le rôle des facteurs confondants
La revue insiste fortement sur les limites méthodologiques des études disponibles. Les indices utilisés pour mesurer l’érosion diffèrent d’une étude à l’autre. Les populations étudiées sont hétérogènes, tant en termes de discipline que de niveau d’entraînement. La définition même de « consommation régulière » varie selon les travaux. Plus important encore, plusieurs facteurs potentiellement déterminants ne sont pas systématiquement contrôlés. Parmi eux, le reflux gastro-œsophagien, l’hygiène bucco-dentaire, le débit salivaire ou encore le régime alimentaire global.
Dans l’une des études incluses, le reflux apparaissait par exemple comme un facteur significativement associé à l’érosion, indépendamment de la consommation de boissons d’effort. Ce point est essentiel, puisque l’environnement acide peut provenir aussi bien de l’extérieur (boisson) que de l’intérieur (reflux gastrique). Cela suggère que les boissons de l’effort ne constituent probablement pas un facteur isolé. Elles s’inscrivent dans un environnement multifactoriel où s’additionnent acidité, fréquence d’exposition, sécheresse buccale et comportements individuels.
Glucides et santé bucco-dentaire en trail et endurance
Une prévalence élevée chez les athlètes
Avant de se focaliser sur le trail et l’ultra-endurance, je vous propose d’aborder une méta-analyse récente sur la prévalence des troubles bucco-dentaires chez les athlètes élite et paralympiques (Mulla et al., 2026). Au total, 34 études ont été incluses, couvrant différentes disciplines sportives et plusieurs pays.
Les résultats montrent que la prévalence des caries était estimée à environ 44 %, celle des maladies parodontales à 47 %, et celle de l’érosion dentaire à près de 30 %. Ces chiffres restent du même ordre de grandeur que ceux observés dans certaines populations adultes générales, suggérant que les athlètes ne semblent ni protégés, ni exposés. Dans la population adulte générale, près de 90 % des adultes âgés de 20 à 64 ans ont déjà présenté au moins une carie dentaire selon les données nationales américaines (National Institute of Dental and Craniofacial Research [NIDCR], 2021).
À l’échelle mondiale, l’OMS estime que plus de 2,3 milliards de personnes vivent avec une carie, en l’une des affections chroniques les plus répandues dans le monde (WHO, 2022). Selon l’Agence Nationale de la Santé Ile-de-France, 33 à 50 % des Français présentent au moins une dent cariée à traiter, et 92% des Français en rencontrent une dans leur vie.
Aussi, une autre question nous intéresse. Qu’en est-il spécifiquement dans les sports d’endurance prolongée, où la fréquence d’exposition aux glucides et la durée d’effort sont particulièrement élevées ? Plusieurs travaux se sont intéressés spécifiquement aux sports d’endurance prolongée. Dans cette section, je vous présente quelques études clés une par une, en décrivant leur méthodologie, leur population et leurs principaux résultats.
Ultra-trail et santé des dents
Coudert et al., 2023
En 2023, Coudert et al. (2023) ont réalisé une étude auprès des participants de l’UT4M. L’objectif était d’évaluer l’état bucco-dentaire des ultra-traileurs et de quantifier leur exposition aux facteurs de risque comportementaux et nutritionnels. Au total, 263 coureurs ont participé à l’enquête. Les auteurs ont analysé l’état de santé orale déclaré, les habitudes alimentaires à l’effort, la fréquence des apports sucrés, ainsi que les comportements préventifs (p. ex. brossage, visites dentaires).
L’exposition aux glucides à l’effort était massive. Plus de 90 % des participants déclaraient consommer régulièrement des produits sucrés pendant la course. Les barres énergétiques étaient consommées par 55 % des coureurs, les gels et confiseries sucrées par 40 %. Le grignotage en dehors des repas concernait près de 40 % de l’échantillon. Malgré cela, 84 % des participants déclaraient une santé bucco-dentaire “bonne” ou “très bonne”. La proportion rapportant une santé bucco-dentaire “mauvaise” restait faible. Sur le plan déclaratif, ces ultra-traileurs ne présentent donc pas pas présenter une situation plus défavorable que la population générale.
Les analyses statistiques montrent que les comportements préventifs jouent un rôle central. Les consultations régulières chez le dentiste étaient significativement associées à une meilleure santé bucco-dentaire déclarée. De plus, la consommation de sucres à l’effort présente une association négative avec la santé bucco-dentaire. Il est important de rappeler que cette étude repose sur des données auto-déclarées, et non sur un examen clinique. Elle ne permet donc pas de mesurer objectivement la prévalence réelle des caries ou de l’érosion.
Doré et al., 2024
En 2024, Doré et al. (2024) ont approfondi la question sous un angle différent, en étudiant les comportements de prévention bucco-dentaire des ultra-traileurs, notamment la fréquence des visites dentaires et leur caractère préventif ou curatif. L’étude a été menée auprès de 263 participants inscrits à l’UT4M. Les chercheurs se sont intéressés à la nature de la dernière visite chez le dentiste (prévention ou traitement) et au délai depuis la dernière consultation (moins d’un an ou plus d’un an).
Les résultats montrent que 62 % des coureurs déclaraient que leur dernière visite avait un objectif préventif, et 60 % avaient consulté un dentiste au cours de l’année écoulée. Au total, 37 % cumulaient à la fois une visite récente et une démarche préventive structurée. Les analyses montrent que les coureurs déclarant un état bucco-dentaire “très bon” avaient une probabilité nettement plus élevée de consulter à titre préventif. De plus, le fait d’avoir consulté dans l’année augmentait significativement la probabilité que la visite soit préventive. Le brossage régulier était lui aussi associé à une démarche préventive.
En revanche, l’exposition déclarée aux sucres à l’effort ne semblait pas associée au recours à la prévention dentaire. Les auteurs observent également que la fréquence annuelle de participation aux courses d’ultra-endurance était associée à une probabilité plus élevée d’avoir consulté récemment, suggérant que les coureurs les plus investis dans leur pratique adoptent davantage de comportements de suivi médical. Il faut cependant rappeler qu’il s’agit de données auto-déclarées, sans examen clinique direct.
Tauler et al., 2024
En 2014, Tauler et al. (2014) ont étudié les modifications de plusieurs marqueurs salivaires en réponse à deux épreuves d’ultra-endurance, à savoir un ultra-trail de 104 km et une épreuve de nage en eau libre de 25 km. L’objectif était d’évaluer différents paramètres physiologiques, dont les variations du débit salivaire.
À l’issue de l’ultra-trail, le débit salivaire diminuait significativement (−15 %). À l’inverse, lors de l’épreuve de nage, le débit salivaire augmentait dans le groupe évoluant à allure modérée, probablement en lien avec l’exposition prolongée à l’eau salée, connue pour stimuler la sécrétion salivaire.
De manière intéressante, sur les deux formats, une diminution significative de l’IgA salivaire était observée. L’IgA est une immunoglobuline présente dans les muqueuses, jouant un rôle majeur dans la défense locale contre les agents pathogènes. Sa diminution transitoire après un effort prolongé est classiquement interprétée comme un marqueur de stress immunitaire aigu.
Comment prévenir les carries chez les sportifs ?
En 2018, Frese et al. (2018) ont publié un RCT sur quatre ans. Leur projet viser à évaluer la gestion et la prévention des caries chez des athlètes pratiquant au moins cinq heures d’endurance par semaine. Cinquante-quatre participants ont été inclus et randomisés en deux groupes. Un groupe test utilisait des produits d’hygiène contenant du fluorure stanneux, tandis que le groupe contrôle utilisait un dentifrice fluoré conventionnel. Tous les participants bénéficiaient en plus d’un suivi structuré, comprenant des examens semestriels, un nettoyage professionnel et des conseils d’hygiène bucco-dentaire.
L’évaluation des caries reposait sur le système ICDAS-II, qui permet de distinguer différents stades de lésions, des atteintes initiales de l’émail jusqu’aux lésions cavitaires profondes. Au cours des quatre années de suivi, le nombre moyen de surfaces dentaires saines augmentait significativement, passant d’environ 65 surfaces à plus de 72. Parallèlement, les surfaces présentant des lésions superficielles et intermédiaires diminuaient significativement.
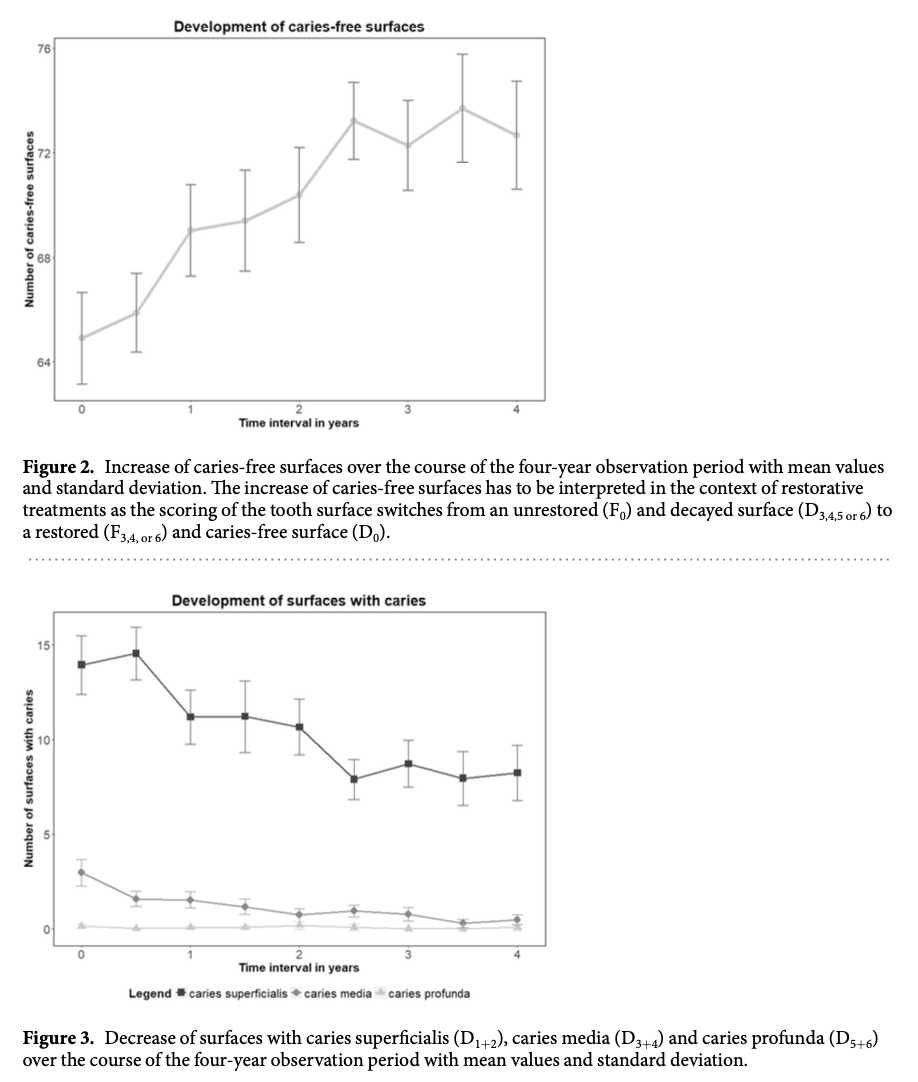
Les analyses statistiques montrent un effet significatif du temps de suivi, traduisant une amélioration progressive de l’état dentaire au fil de l’intervention. En revanche, l’utilisation spécifique de produits au fluorure stanneux ne montrait pas d’effet supplémentaire significatif par rapport aux produits fluorés conventionnels. De plus, les résultats indiquent qu’après quatre ans, le risque de développer une nouvelle lésion de type “caries media” (atteinte s’étendant à la dentine) était environ 25 fois plus faible qu’à l’inclusion.
Cette étude suggère qu’un encadrement préventif régulier et structuré peut compenser les risques potentiels associés à la consommation fréquente de produits glucidiques à l’effort.
Les recommandations en nutrition sportive sont-elles dangereuses pour nos dents ?
Mais alors, les recommandations en nutrition sportive sont-elles dangereuses pour nos dents ? Cette question est posée explicitement par Broad et Rye en 2015. C’est même le titre de leur article. Ces auteurs ne remettent pas en cause les fondements physiologiques des recommandations actuelles en nutrition d’endurance. Ils reconnaissent que l’augmentation de l’apport en glucides, la fréquence d’ingestion et l’utilisation de produits spécifiques sont cohérentes avec les exigences énergétiques des sports d’endurance.
Leur question est donc plus subtile : dans quelles conditions ces recommandations peuvent-elles entrer en conflit avec la santé bucco-dentaire ?
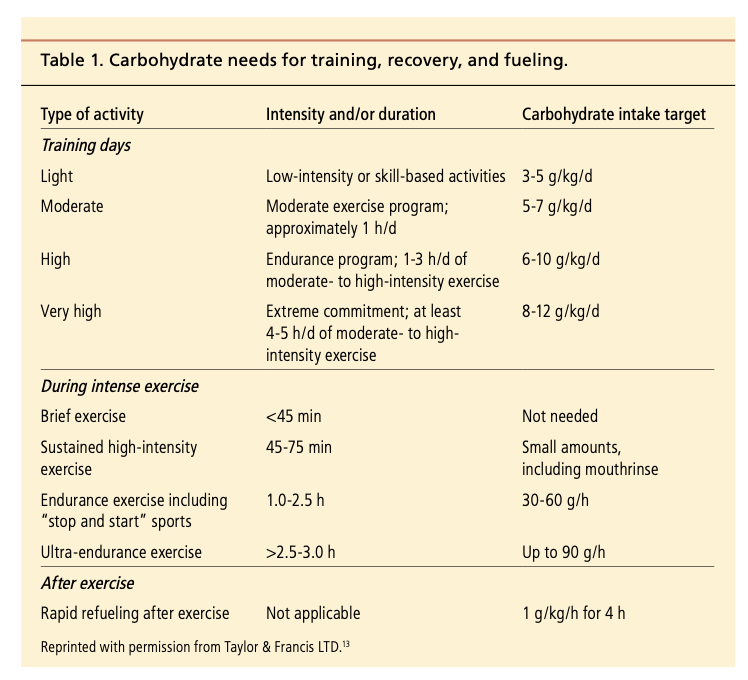
Les auteurs soulignent que le risque potentiel repose principalement sur trois paramètres :
- L’augmentation de la fréquence d’exposition aux glucides fermentescibles.
- Le temps de contact entre les produits sucrés ou acides et la surface dentaire.
- L’acidité intrinsèque de nombreuses boissons sportives.
À cela s’ajoute un facteur spécifique à l’athlète, la déshydratation. Celle-ci réduit le débit salivaire et diminue les capacités de tamponnement, de clairance des sucres et de reminéralisation. Autrement dit, ce ne sont pas les recommandations qui pose problème, mais leur interaction avec un environnement buccal temporairement fragilisé. L’ingestion répétée de boissons acides dans un contexte de bouche sèche peut créer des conditions favorables à l’érosion ou à la carie, en particulier chez les individus déjà susceptibles.
Les stratégies qui aident pour protéger ses dents
Cependant, Broad et Rye (2015) insistent sur le fait que ce risque peut être largement modulé. L’identification précoce des facteurs de vulnérabilité individuelle, un examen bucco-dentaire avant l’engagement dans un programme d’entraînement intensif, l’utilisation régulière de fluor topique, ainsi que des stratégies simples comme le rinçage à l’eau après ingestion de produits sucrés ou acides permettent de réduire significativement l’impact potentiel. Les auteurs défendent également l’idée d’une collaboration entre dentistes et diététiciens du sport, afin d’adapter les stratégies nutritionnelles aux contraintes bucco-dentaires individuelles.
Lles recommandations en nutrition sportive ne seraient donc pas incompatibles avec la santé orale. Elles nécessitent simplement une approche intégrée et personnalisée. La réponse à la question posée en 2015 n’est donc ni alarmiste ni rassurante à l’excès. Les recommandations actuelles ne sont pas intrinsèquement dangereuses pour les dents. Elles exigent simplement que la prévention bucco-dentaire fasse partie intégrante de la stratégie de performance.
Conclusion – Les gels et boissons d’effort détruisent-ils vos dents ?
Au terme de cette revue, une idée ressort. Les recommandations glucidiques en endurance ne “détruisent” pas mécaniquement les dents. Cependant, ces produits peuvent augmenter l’exposition à certains risques lorsque l’on cumule fréquence d’ingestion, acidité des boissons et baisse transitoire des défenses naturelles de la bouche (salive, hydratation). Les données disponibles, y compris chez les ultra-traileurs, ne pointent pas vers une catastrophe généralisée, mais vers un risque multifactoriel, dépendant des comportements (hygiène, prévention, suivi dentaire) et des susceptibilités individuelles.
La conclusion pratique est donc simple : la performance ne doit pas opposer la santé bucco-dentaire, elle doit l’intégrer. Comme le défendent Broad et Rye (2015), la stratégie la plus efficace n’est pas de renoncer aux glucides, mais de sécuriser leur utilisation par une prévention structurée, des habitudes cohérentes, l’utilisation de produits protecteurs adaptés, et un suivi régulier.
Découvrez cet article en podcast !
Partie 1 – Mes explications
En podcast vidéo
En podcast audio
Partie 2 – Mon interview d’un experte – Anne-Charlotte Bas
En podcast vidéo
En podcast audio
Références bibliogaphiques
• Broad, E. M., & Rye, L. A. (2015). Do current sports nutrition guidelines conflict with good oral health. Gen Dent, 63(6), 18-23.
• Coudert, S., Jacq, R., & Bas, A. C. (2023). The evaluation of oral and dental health and behavioural risk among ultra-endurance athletes: a cross-sectional epidemiological study. Research in Sports Medicine, 31(6), 802-810.
• Doré, A., Jacq, R., & Bas, A. C. (2024). Athletes’ medical preventive behaviors: the case of oral health and ultraendurance trail runners. BMC Oral Health, 24(1), 777.
• Dubois, M., Delcourt, B., Ortis, M., Bougault, V., Doglio, A., Bertrand, M. F., … & ORTIS, M. (2025). Correlation Between the Oral Microbiota and Sports Practice: A Systematic Review. Cureus, 17(1).
• Engels-Deutsch, M. (2026). The bacterial flora of the mouth and its impact on athletic performance and general health. Research in Sports Medicine, 34(1), 11-26.
• Frese, C., Frese, F., Kuhlmann, S., Saure, D., Reljic, D., Staehle, H. J., & Wolff, D. (2015). Effect of endurance training on dental erosion, caries, and saliva. Scandinavian journal of medicine & science in sports, 25(3), e319-e326.
• Frese, C., Wohlrab, T., Sheng, L., Kieser, M., Krisam, J., Frese, F., & Wolff, D. (2018). Clinical management and prevention of dental caries in athletes: A four-year randomized controlled clinical trial. Scientific reports, 8(1), 16991.
• Glick, M., Williams, D. M., Kleinman, D. V., Vujicic, M., Watt, R. G., & Weyant, R. J. (2016). A new definition for oral health developed by the FDI World Dental Federation opens the door to a universal definition of oral health. British dental journal, 221(12), 792-793.
• Memon, M. A., Khan, M. A., Ahmad, M., Tariq, I., Younus, K., Aleem, B., & Lee, K. Y. (2025). Sports Drinks and Dental Erosion: Unveiling the Evidence from a Systematic Review. Current Oral Health Reports, 12(1), 1-10.
• Moynihan, P., & Petersen, P. E. (2004). Diet, nutrition and the prevention of dental diseases. Public health nutrition, 7(1a), 201-226.
• Mulla, M., Langaliya, A., Jawahar, A., Mulla, M., Galletti, C., Mathur, A., & Fiorillo, L. (2026). Global Prevalence and Patterns of Oral Health Disorders in Elite and Paralympic Athletes: A Systematic Review and Meta-Analysis. Journal of Craniofacial Surgery, 10-1097.
• National Institutes of Health. (2008). Dental caries (tooth decay) in adults (age 20 to 64).
• Tauler, P., Martinez, S., Moreno, C., Martínez, P., & Aguilo, A. (2014). Changes in salivary hormones, immunoglobulin A, and C-reactive protein in response to ultra-endurance exercises. Applied Physiology, Nutrition, and Metabolism, 39(5), 560-565.



